2024年9月25日,鼎科医疗技术(苏州)有限公司(以下简称“鼎科医疗”)宣布,其自主研发的DKutting™ LL外周刻痕球囊扩张导管正式获得国家药品监督管理局(NMPA)批准上市(国械注准20243031906)。
外周血管疾病治疗的新利器
随着我国老年人口的不断增加,外周血管疾病患者数量也在持续上升。据预测,到2030年,中国外周动脉疾病患者总数将达到6,230万人。随着“介入无植入”的理念被广泛接受,保障药涂球囊长期效果的“血管准备”愈发受到关注,DKutting™ LL定向刻痕球囊作为充分预处理的利器而生,将为下肢动脉介入提供一种全新的治疗选择。
独家技术 为下肢介入而生
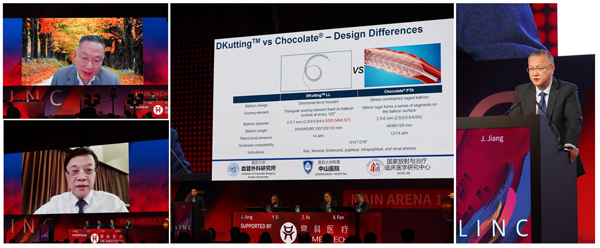
DKutting™ LL沿用鼎科医疗独创的三角形镍钛绕簧专利技术,结合下肢动脉的实际临床需求,大幅增加了刻痕件长度(最长达150mm),并研发了全新的兼容0.014”/0.018”导丝的完全同轴球囊输送系统,并以0.5mm间隔丰富了球囊直径的选择。鼎科医疗独有的定向刻痕球囊,具备径向强劲扩张和轴向灵动过弯的综合性能,其临床表现在冠脉领域和血透通路领域已经获得充分认可。最新研发的DKutting™ LL刻痕球囊针对下肢动脉介入专门设计,在定向扩张机制上展现出显著的临床优势,定义了外周血管预扩的新标准。
重磅RCT临床研究
由复旦大学附属中山医院血管外科符伟国教授牵头的 DELTA研究(clinicaltrials.gov ID NCT05608655),是全球最大规模的外周特殊球囊对照研究,也是全球第一个对照美敦力公司Chocolate® 球囊的头对头研究。在LINC2024全球首发的研究结果显示:DKutting™ LL刻痕球囊在降低夹层发生风险率和支架补救率方面与对照组相似,在管腔获得和减少残余狭窄方面表现更佳。通过DELTA研究结果显示:DKutting™ LL刻痕球囊同时具备“高扩张力”与“低损伤性”的双重特性,必将成为“血管准备”首选泛用性球囊。
挑战国际金标准
确立预扩新标准DKutting™ LL刻痕球囊诞生于中国,服务于全球患者,将成为下肢动脉预处理的重要器械。
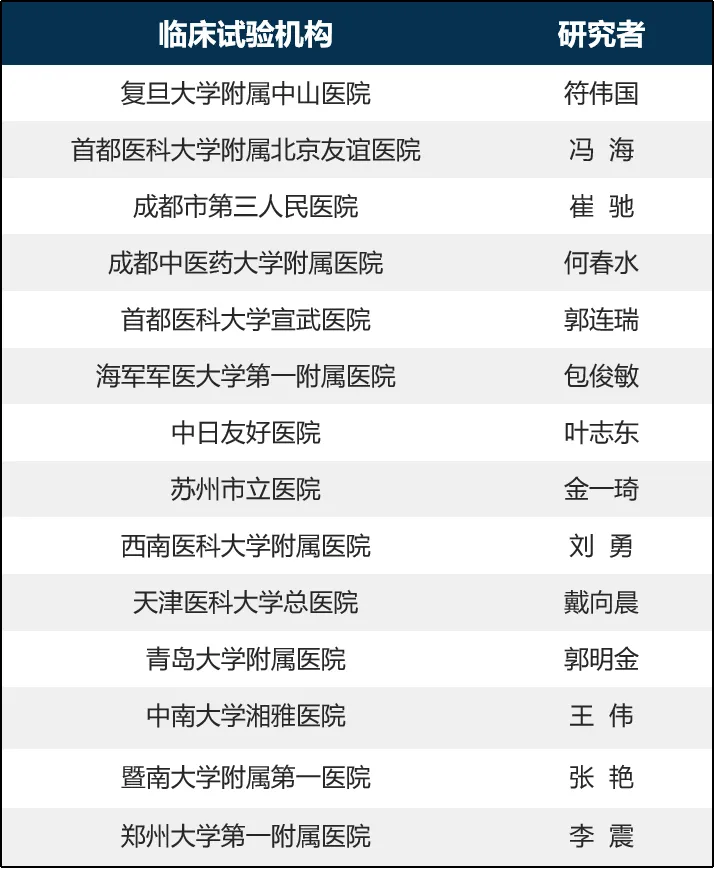
DELTA研究临床中心